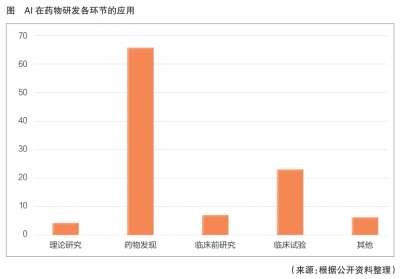
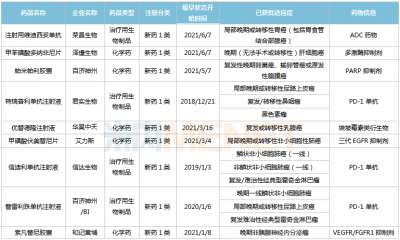
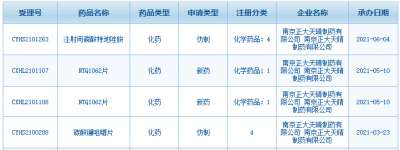
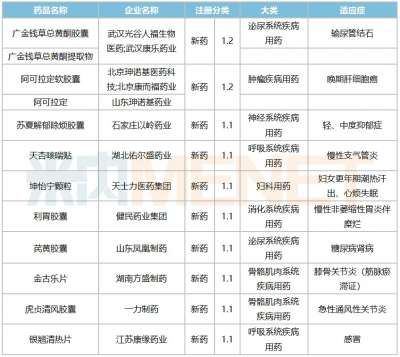
2020全年审评通过创新药20个 审评资源向具有明显临床价值创新药品和急需药品倾斜
医药网6月23日讯 国家药监局6月21日发布《2020年度药品审评报告》。《报告》显示,2020全年审评通过创新药20个。 《报告》显示,全年有59件新冠病毒疫苗和新冠肺炎治疗药物的注册申请被纳入特别审批程序并完成技术审评。受理1类创新药注册申请共1062件(597个品种),较2019年增长51.71%。审评通过新药上市申请208件,较2019年增长26.83%。审评通过创新药上市申请20个品种(1类化学药14个、中药创新药4个、创新生物制品2个)。审评通过境外生产原研药品新药上市申请72个品种(含新增适应症品种)。 在突破性治疗药物程序方面,药审中心审评通过的新药上市申请中,共有15件申请经附条件批准后上市。在药品加快上市注册程序下,审评资源向具有明显临床价值的创新药品和急需药品倾斜。譬如,纳入优先审评审批程序的注册申请包括42件儿童用药和罕见病用药,经附条件批准上市的药品覆盖新型冠状病毒感染引起的疾病、非小细胞肺癌等适应症。